Ösophagus
von: Christoph Fischer
Suchbegriffe: Reflux, GERD, Barettösophagus, Ösophaguskarzinom, Ösophagus-Ca, Reflux-Thoraxschmerz-Syndrom, H. pylori-Eradikation, PPI-Dauer-Therapie, Reflux-Thoraxschmerz-Syndrom, intestinaler Metaplasie, Becherzellen, spezialisiertes Zylinderepithel,
Häufigkeit: Refluxbeschwerden sind sehr häufig: 1 von 5 Erwachsenen leidet an GERD, aber pro Jahr erkrankt nur 1 von 11.000 Männern und 1 von 50.000 Frauen an Ösophagus-Ca. Deshalb soll sich die Magenspiegelung auf Riikopatienten beschränken!
Risiko: pro Jahr erkrankt 1 von 200 Patienten mit Barett-Ösophagus mit intestinaler Metaplasie an Ösophagus-Ca
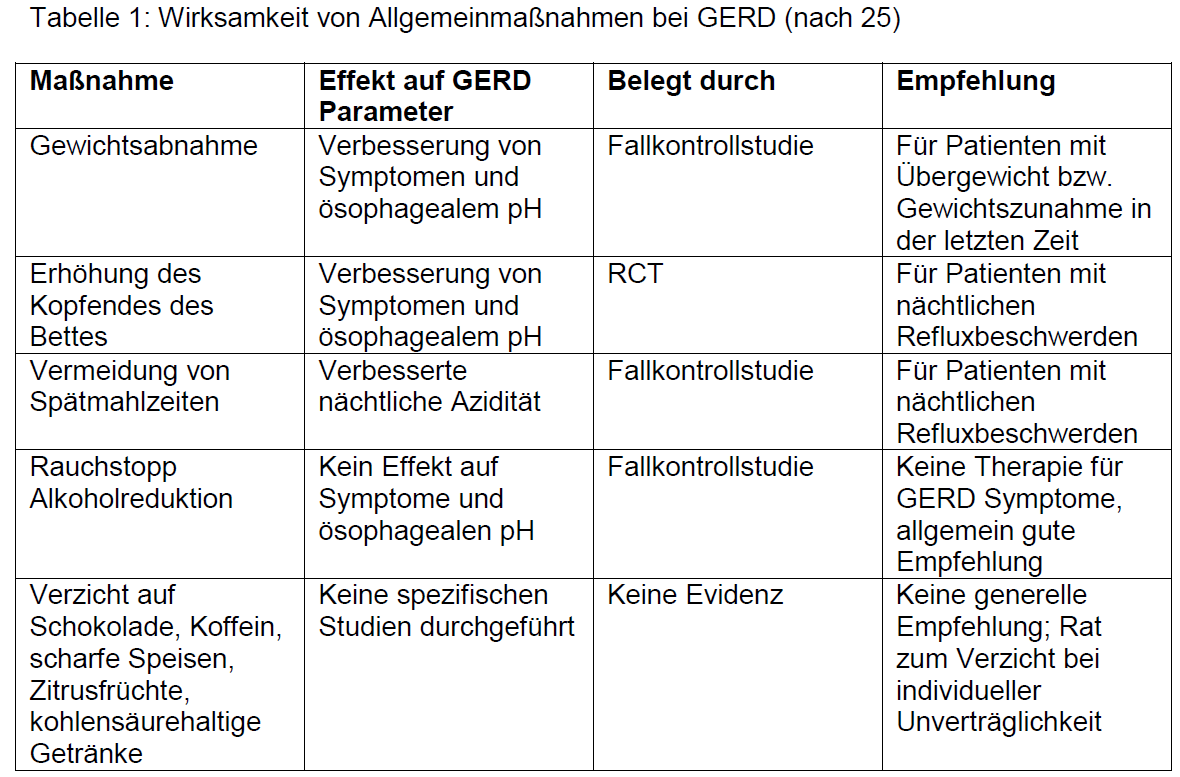
Warn-Hinweis: Schlafmittel (z.B. Zolpidem) können zu einer Verschlechterung des nächtlichen Refluxes führen.
empirische medikamentöse Therapie
|
Patienten mit typischen Refluxsyndrom ohne Alarmzeichen oder Risikofaktoren
|
|
Management-Algorithmus zur Abklärung und Therapie typischer Refluxbeschwerden |
HintergrundINFO: 40-80% der Schwangeren leiden an GERD, Risiken einer PPI-Behandlung in der Schwangerschaft sind bisher nicht gesichert, können aber auch nicht mit an Sicherheit grenzender Wahrscheinlichkeit ausgeschlossen werden.
Indikation zur Gastroskopie
| Bei mehrjährig bestehenden Refluxbeschwerden, Alarmzeichen oder Risikofaktoren sollte eine Endoskopie zur Aufdeckung eines Barrett-Ösophagus erfolgen. S-2LL S: 17 |
HintergrundINFO: Die makroskopischen Läsionen sind derart spezifisch, dass mit ihrem Nachweis die Diagnose "Refluxösophagitis" ausreichend belegt ist. Aus den Befunden der pH-Metrie und Ösophagusmanometrie lassen sich zunächst keine differenzialtherapeutischen Konsequenzen ableiten.
- Bei symptomatischer Refluxösophagitis wird daher ohne weitere Funktionsdiagnostik medikamentös therapiert.
- Eine Biopsie bei makroskopisch unauffälligen Ösophagus nur zur Klärung der Frage einer Refluxerkrankung sollte nicht durchgeführt werden. 2S-LL S: 20
Therapie nach Gastroskopiebefund
Algorithmus zum Langzeit-Management der GERD nach Schweregrad |
Helicobacter pylori und GERD
| die H. pylori-Eradikation ist einer Langzeittherapie mit einem PPI vorzuziehen, um einer Zunahme der Corpusgastritis und einer beschleunigten Atrophie-Entwicklung vorzubeugen |
Reflux-Thoraxschmerz-Syndrom
|
HintergrundINFO: Thoraxschmerzen, die von einem ischämischen Herzschmerz klinisch nicht zu unterscheiden sind, können Symptom einer GERD sein, ohne dass typische Refluxsymptome wie Sodbrennen oder Regurgitation vorliegen. Eine Probetherapie mit einem PPI bei vermutetem Reflux-Thoraxschmerz-Syndrom ist zur Diagnostik geeignet.
Risiko PPI-Dauer-Therapie
|
HintergrundINFO: bei reduzierter Säuresekretion kolonisiert H. pylori bevorzugt die Corpusschleimhaut des Magens mit der Konsequenz einer Zunahme der Corpusgastritis und gleichzeitiger Verbesserung der Antrumgastritis. Kuipers et al, die zwei Kohorten von Refluxpatienten behandelt mit PPI-Dauertherapie oder Fundoplicatio verglichen, folgerten, dass eine PPI-Dauertherapie die Atrophieentwicklung bei bestehender HP-Infektion beschleunigt und damit evtl. das Magenkarzinomrisiko langfristig erhöht.
Chirurgische Therapie
|
Der Therapieerfolg einer PPI-Therapie ist vergleichbar mit dem einer laparoskopischen Fundoplikatio.Eine Operationsindikation kann gestellt werden, wenn zusätzlich zur langfristigen Behandlungsbedürftigkeit die Indikationskriterien erfüllt sind:
Refluxrezidive nach Fundupltkatio ohne weitere komplizierende Faktoren sollten zunächst wieder mit PPI behandelt werden. |
extraösophageale Manifestationen der GERD (EÖM)
|
Mögliche extraösophageale Manifestationen einer GERD sind
bei Verdacht auf EÖM sollte eine empirische PPI-Therapie versucht werden |
HintergrundINFO: Ein etablierter Diagnostikalgorithmus zur Abklärung einer EÖM existiert nicht. Aufgrund des schlechteren Therapieansprechens bei Symptomen der
EÖM im Vergleich zu typischen GERD-Symptomen ist ein objektivierter Nachweis der
Refluxkrankheit vor Beginn der medikamentösen Therapie prinzipiell wünschenswert. Die Evidenz aus Therapiestudien ist widersprüchlich
Barett-Ösophagus
|
HintergrundINFO: Das Risiko der Progression eines nicht-neoplastischen Barrett-Ösophagus hin zur hochgradigen intraepithelialen Neopalsie oder Adenokarzinom ist äußerst niedrig, diesem steht das Komplikationsrisiko einer ablativen Therapie entgegen.
Die gesicherte niedriggradige intraepitheliale Neoplasie ist eine relevante Erkrankung mit hoher Progressionsrate.
Die Diagnose einer niedriggradigen intraepithelialen Neoplasie (LGIN) muss immer durch einen erfahrenen Referenzpathologen überprüft werden, da es sich in 85% der Fällen um eine Fehldiagnose handelt (Fehlinterpretation entzündlicher Veränderungen als neoplastisch)
Prävention Ösophagus-Ca
| Eine Empfehlung zur Prävention der Entwicklung von Neoplasien im Barrett-Ösophagus (PPI, ASS) kann nach heutigem Kenntnisstand nicht abgegeben werden. PPI führten lediglich zur Reduktion akuter entzündlicher Veränderungen, während chronische entzündliche Veränderungen persistierten. |
Literatur:
(1)[1] Ka Shing Cheung, Wai Keung Leung et al., Long-term proton pump inhibitors and risk of gastric cancer development after treatment for Helicobacter pylori: a population-based study, https://gut.bmj.com/content/67/1/28
